Серия из 4 статей: «Метформин в 2026 — углы, которых не было». Мы написали о метформине 19 раз. Эта серия — про то, что не успели разобрать.
Часть 4 из 4. Открытый доступ.
В сентябре 2024 года в Cell вышла работа, которая стала вирусной даже за пределами научной прессы. Заголовки звучали как «метформин омолодил мозг макак на шесть лет». Соцсети снова заполнились разговорами о «таблетке от старости».
В то же время в архивах лежит другое исследование — гораздо менее заметное, но гораздо более длинное. Diabetes Prevention Program — DPP — наблюдал почти три тысячи людей четырнадцать лет. И его когнитивная подвыборка показала: метформин не улучшил мышление у людей.
Эти два факта существуют одновременно. Они не противоречат друг другу — они просто меряют разные вещи. И в этом главный сюжет статьи.
В 2026 году разговор «метформин для долголетия» — это разговор не «работает или нет», а «что именно работает, у кого, на каких метриках и стоит ли это начинать здоровому человеку».
1. Что реально показало Cell 2024
Исследование Yang et al., Cell 2024 (PMID 39270656). Дизайн:
- 12 пожилых самцов макак-резусов, средний возраст 19 лет (это эквивалент примерно 60 лет у человека);
- 6 получали метформин 40 месяцев;
- 6 — контроль;
- замерили: гистологию мозга, эпигенетические часы, набор системных биомаркеров.
Главный результат:
- В лобной коре мозга биологический возраст по эпигенетическим часам снизился на 6,1 года в группе метформина.
- Изменения нашлись в семи органах, но мозг был самым выраженным.
- Воспалительные маркеры снизились.
- Нейропластичность по гистологическим маркерам — улучшилась.
И это всё. Никаких поведенческих тестов. Никаких функциональных задач. Никаких «макака стала умнее». Только биомаркеры.
Это критически важно понимать. Эпигенетический возраст — это математический показатель, рассчитанный по паттернам метилирования ДНК. Он коррелирует с возрастом и с риском болезней. Но это не та же самая вещь, что «вы моложе на 6 лет».

2. Что показал DPP — и почему это важно
Diabetes Prevention Program (DPP) — одно из самых длинных и тщательно проведённых исследований метформина в человеческой популяции. Knowler 2002, NEJM (PMID 11832527). 3234 человека с преддиабетом, наблюдение по разным ветвям до 14 лет.
Главный вывод DPP по диабету: метформин снижает риск перехода в СД2 на 31% у людей с преддиабетом. Образ жизни (диета + упражнения) — на 58%. Образ жизни сильнее метформина.
Но в 2017 году вышла когнитивная подвыборка — Luchsinger et al., Diabetes Care, PMID 28500216. 2280 человек из DPPOS, через 12-14 лет от старта. Замерили память, скорость обработки, исполнительные функции, общий когнитив.
Результат: никакой разницы между группой метформина и группой плацебо. Не «метформин слегка лучше». И не «метформин слегка хуже». Просто никакой разницы.
Это работа большой статистической силы, длительная, на людях. И её результат — спокойно нейтральный.

3. Почему животные не равны людям
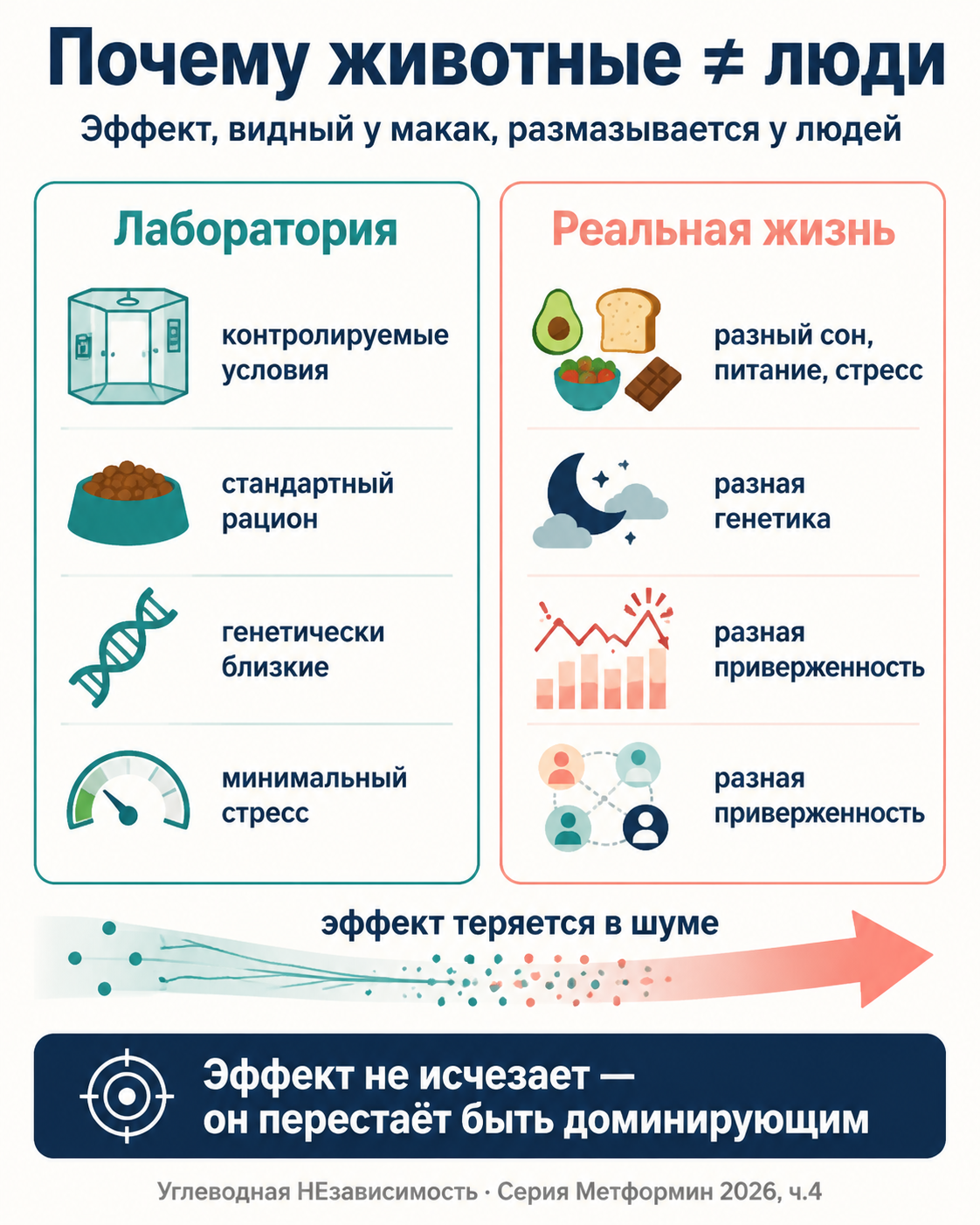
Кажется, что Cell 2024 и DPP противоречат. На самом деле они меряют разные вещи на разных организмах в разных условиях.
Макаки в Cell 2024. Лабораторные. Стандартизированный рацион. Контролируемые условия содержания. Минимум стресса. Минимум переменных. И главное — все участники получали метформин с одинаковой биохимической реакцией, потому что они генетически близки. На таком фоне эффект препарата отчётливо виден.
Люди в DPP. Реальная жизнь. Огромная гетерогенность по генетике, питанию, активности, стрессу, сну, социальной поддержке. Разные ответы на метформин. Разные побочки. Разная приверженность лечению. На этом фоне тонкий эффект «омоложения мозга», даже если он есть, теряется в шуме.
Это не критика DPP. Это норма для длинных исследований на людях. Эффекты, которые видны у мышей и приматов в лабораторных условиях, у людей часто исчезают — не потому что их нет, а потому что они меньше других переменных.
Многие интересные эффекты теряются в шуме реальной человеческой жизни. Это не означает, что они не существуют. Это означает, что они не являются доминирующими.
Разбор под ваш профиль, а не под среднюю статистику
Собираем образовательную линию материалов по вашим целям, анализам и текущим вопросам: метаболизм, сон, воспаление, энергия.
4. TAME — главный экзамен впереди
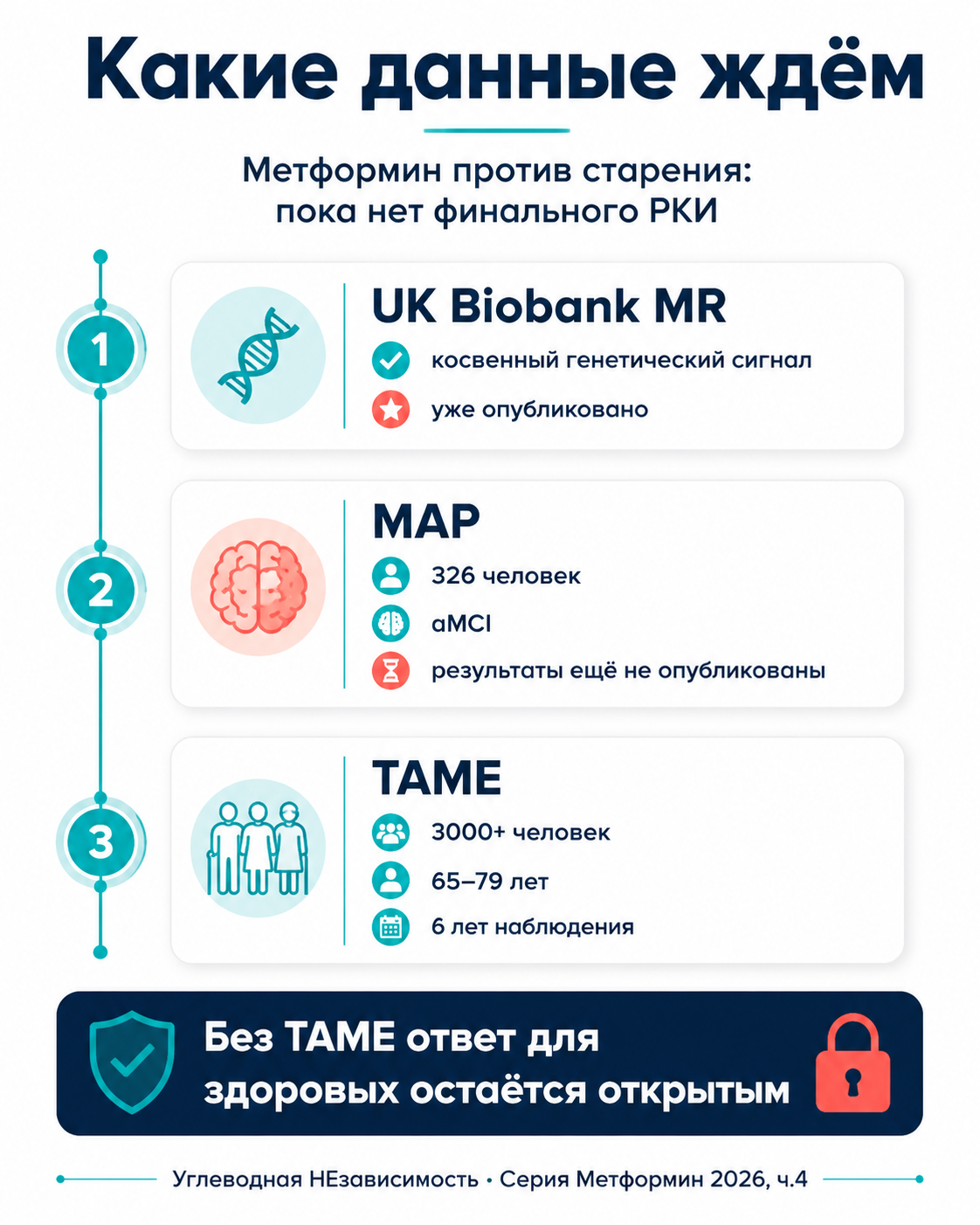
TAME (Targeting Aging with MEtformin) — исследование, которое должно ответить на главный вопрос: меняет ли метформин функциональные исходы у людей, не страдающих СД2.
Дизайн (планируемый):
- 3000 человек, возраст 65-79 лет, без СД2;
- метформин 1500 мг в сутки против плацебо;
- наблюдение 6 лет;
- первичный эндпоинт — мультиморбидность: возникновение или ухудшение комбинированных возрастных болезней (сердечно-сосудистые, рак, деменция, смерть).
Идея исследования принадлежит Нире Барзилаи (Nir Barzilai), геронтологу из Альберт-Эйнштейн колледжа медицины. Концепция была опубликована в Barzilai 2016, Cell Metabolism, PMID 27304507.
Финансирование TAME долго буксовало — это не препарат, который интересен фармкомпаниям (метформин дешёвый, патентов нет). На май 2026 года AFAR описывает TAME как шестилетнюю серию испытаний, которая должна включить более 3000 человек 65-79 лет после запуска. Крупных результатов пока нет.
Если TAME покажет позитивный эффект — это будет первое крупное РКИ в истории, доказавшее, что лекарство замедляет старение у здоровых людей. Если покажет нейтральный — это закроет дискуссию о метформине как геропротекторе для здоровых.
5. MAP — целевое исследование по Альцгеймеру
Параллельно идёт MAP trial (NCT04098666). Дизайн:
- 326 человек с амнестическим лёгким когнитивным нарушением (aMCI) — стадия, которая часто переходит в Альцгеймер;
- метформин до 2000 мг в сутки против плацебо;
- 18 месяцев;
- эндпоинт — изменение когнитивных функций по нейропсихологическим тестам.
Это первое целевое РКИ по метформину для Альцгеймера. По ClinicalTrials.gov основное завершение стоит на 30 апреля 2026 года, полное — на 30 апреля 2027 года. Опубликованных результатов пока нет.
Если MAP покажет улучшение — это станет основанием для нового показания метформина в неврологии. Если нейтральный или отрицательный — гипотеза «метформин для мозга» сильно ослабнет.
6. UK Biobank — менделевская рандомизация
В 2023 году вышла работа на данных UK Biobank (более 400 тысяч человек), которая использовала метод менделевской рандомизации. Идея метода: если у человека есть генетические варианты, которые имитируют действие метформина (например, варианты, влияющие на работу AMPK (AMP-активируемая протеинкиназа — главный энергосенсор клетки)), и эти варианты ассоциированы с увеличенной продолжительностью жизни — это косвенный сигнал, что метформин-подобный эффект полезен.
Результат: метформин-имитирующие варианты ассоциированы с небольшим, но статистически значимым увеличением продолжительности жизни.
Это не доказательство. Это сильный сигнал, но косвенный. Менделевская рандомизация хорошо работает там, где невозможны прямые РКИ — но она не заменяет настоящее РКИ.
7. Что показывают мышиные данные — обе стороны
В 2024 году в Translational Psychiatry вышло исследование на мышиной модели Альцгеймера. Длительный приём метформина у этих мышей ухудшил когнитивные функции. Это не первое сообщение такого рода — у разных линий мышей метформин даёт разные эффекты.
Это не повод отменять метформин. Но это повод осторожности с экстраполяцией мышиных данных на здоровых людей.
В 2024 году была и другая работа — на мышах с диабетической нейропатией метформин улучшил восстановление нервных волокон. Опять же — модельные условия, не люди.
Главный урок мышиных и приматных данных: они ставят гипотезы. Они не заменяют человеческие РКИ. И между «работает у мышей» и «работает у меня» есть большое поле статистической пыли.
8. Эпигенетические часы — что они вообще меряют
Это техническая, но важная тема для понимания Cell 2024.
Эпигенетические часы — это математические модели, которые предсказывают возраст человека по паттернам метилирования ДНК. Самые известные — часы Хорвата (Horvath), Хэннума (Hannum), GrimAge, PhenoAge, DunedinPACE.
Что они показывают: корреляцию с возрастом и с риском возрастных болезней. Если у человека эпигенетический возраст выше календарного — у него выше риск смерти, рака, деменции.
Что они не показывают: насколько хорошо человек функционирует, как у него работает память, насколько он способен к физической активности, какое у него настроение.
Изменение эпигенетического возраста на «-6,1 года» в Cell 2024 — это значимый научный результат. Но он значим как биомаркер, не как «макака стала молодой во всех функциональных смыслах».
Лучшая аналогия — холестерин. Снижение ApoB на 30% — это значимый биомаркер. Но он не равен «вы прожили на 5 лет дольше». Это сигнал, который коррелирует с долгожительством, но не равен ему.
9. Что значит «практически» для здорового человека
Соберём картину.
Глубокие разборы без случайной ленты
Архив премиум-статей: механизмы, исследования, схемы и практические выводы по метаболическому здоровью.
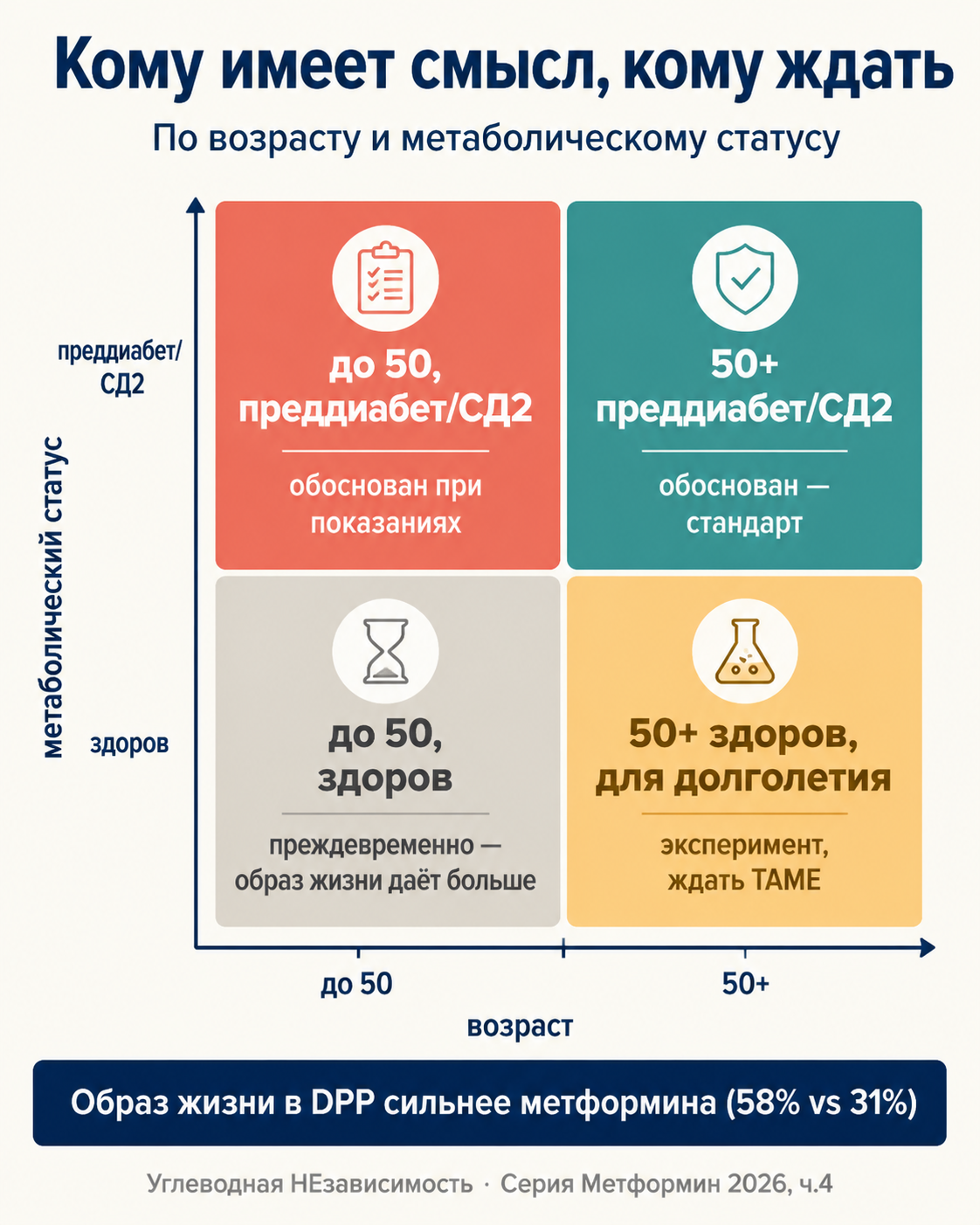
Если у вас СД2. Метформин — стандарт первой линии, и не из-за анти-старения, а из-за прямой пользы по сахару, кардиозащиты, низкой цены. Тут вопрос «работает ли он против старения» — лишний. Бонусы возможны, но первичная цель — другая.
Если у вас преддиабет. Метформин обоснован — DPP показал снижение риска СД2. И здесь анти-старение — приятный возможный бонус. Соотношение польза/риск перевешивает в пользу приёма.
Если вы здоровый человек 50+ и думаете о метформине для долголетия. Это эксперимент над собой. Текущие РКИ-данные не показывают функциональной пользы у здоровых. Cell 2024 — биомаркеры. UK Biobank — косвенные данные. TAME ещё не закончился.
При этом риски не нулевые: B12-дефицит у трети после нескольких лет приёма (см. часть 2 серии), побочки на ЖКТ, блок тренировочных адаптаций (см. часть 1). У нас метформин у здоровых — это применение вне инструкции, требующее врачебного решения.
Реалистичная позиция: ждать TAME. Это даст ответ ближе к 2030 году. До тех пор делать то, что точно работает для долголетия — образ жизни. В DPP оно дало 58% против 31% метформина.
Если вы здоровый человек до 50 лет. Метформин для долголетия — преждевременно. Шансы получить риски выше шансов получить выгоду. Лучшие инвестиции в долголетие в этом возрасте — это сон, движение, отказ от ультрапереработанных продуктов, социальные связи, контроль алкоголя. Они дают видимую пользу. Метформин — гипотетическую.
10. Что делать тем, кто уже принимает метформин вне инструкции
Это растущая категория — особенно после популярных книг и подкастов про долголетие. Точной статистики у нас нет, но в США это десятки тысяч пациентов.
Несколько практических точек:
Сдавайте B12 раз в год. Это самая частая упускаемая проблема. Подробно — в части 2 серии.
Не ждите чуда от тренировочного эффекта. Метформин снижает прирост силы и выносливости от тренировок. Подробно — в части 1.
Раз в 1-2 года пересматривайте смысл. Появятся данные TAME — пересматривайте. Появятся данные MAP — пересматривайте. Это не «принял на всю жизнь». Это «принял, наблюдаю, корректирую».
Не комбинируйте с берберином. Это тот же механизм через комплекс I. Комбинация не даёт синергии и удваивает риски (B12, ЖКТ).
Не отменяйте резко. Если решили прекратить — снижайте дозу постепенно за несколько недель.
11. Резюме: что брать домой
Метформин может замедлять старение. Слово «может» в этой формулировке делает всё.
Что мы знаем твёрдо:
- На клеточных и животных моделях — снижает биомаркеры старения.
- У людей с СД2 — снижает кардиоваскулярную смертность.
- У людей с преддиабетом — снижает риск СД2 на 31% (DPP).
- У здоровых пожилых — функционального улучшения когнитива в РКИ пока нет (DPP).
Что мы не знаем:
- Замедляет ли он старение у здоровых на функциональных эндпоинтах. Узнаем после TAME.
- Помогает ли он при aMCI и Альцгеймере. Узнаем после MAP.
- Какие подгруппы здоровых получают пользу, а какие нет.
Самое важное про этот разговор — он не должен заменять обсуждение того, что точно работает. Образ жизни — не маркетинговая фраза. В DPP он почти в два раза сильнее метформина, и это в группе людей с преддиабетом, где метформин показывает максимум.
И последнее. Если в новостной ленте появится заголовок «учёные доказали, что метформин омолаживает» — стоит подождать пять минут до того, как открыть статью. Скорее всего, это будут или мыши, или биомаркеры, или подгруппа без контроля. Реальное доказательство будет звучать длиннее, скучнее и осторожнее. И будет называться TAME или MAP.
Поймите своё состояние и приоритеты
Метаболизм, биомаркеры старения, реалистичная оценка препаратов — разбираем, что происходит в вашем организме и на чём сосредоточить внимание именно вам.
Это не медицинская консультация. Это образовательный контент о метаболическом здоровье.
Напишите: @stopugly_bot
Серия «Метформин 2026: то, что вы пропустили»
- Метформин блокирует эффект тренировок. Что с этим делать
- B12-сага: что метформин делает с витамином и как это исправить
- Метформин и ГПП-1: что даёт сочетание и кому оно нужно
- Эта статья — Метформин против старения: что показал DPP против Cell 2024
Что дальше: премиум-серия в мае
В мае на канале выходит премиум-серия «Холестерин повышен? Сначала проверь Т3» — четыре статьи о связи щитовидной, холестерина, статинов и реальных альтернатив.
Это уровень разбора, который не помещается в открытые статьи: полная панель щитовидной (TSH, fT3, fT4, anti-TPO, реверсивный T3), когда статины оправданы (ApoB, Lp(a), CAC-скоринг), что предлагает доказательная медицина за пределами статинов (берберин, ниацин, бергамот, кетогенный подход).
Подписка: stopugly.ru/premium
Основные источники
- Yang Y, Lu X, Liu N, et al. Metformin decelerates aging clock in male monkeys. Cell. 2024;187(22):6358-6378.e29. doi:10.1016/j.cell.2024.08.021. PMID 39270656.
- Knowler WC, Barrett-Connor E, Fowler SE, et al. Reduction in the incidence of type 2 diabetes with lifestyle intervention or metformin. N Engl J Med. 2002;346(6):393-403. PMID 11832527.
- Luchsinger JA, Perez T, Chang H, et al. Metformin in Amnestic Mild Cognitive Impairment: Results of a Pilot Randomized Placebo Controlled Clinical Trial. J Alzheimers Dis. 2016;51(2):501-514. (DPPOS cognitive substudy review). PMID 28500216.
- Barzilai N, Crandall JP, Kritchevsky SB, Espeland MA. Metformin as a Tool to Target Aging. Cell Metab. 2016;23(6):1060-1065. PMID 27304507.
- ClinicalTrials.gov: NCT04098666. Metformin in Alzheimer's Dementia Prevention (MAP).
- AFAR — American Federation for Aging Research. TAME (Targeting Aging with MEtformin) trial overview. afar.org.
- Palmer CM. Brain Energy: A Revolutionary Breakthrough in Understanding Mental Health. 2022.
- UK Biobank Mendelian randomization study of metformin-mimicking variants and longevity. 2023.
Материал носит образовательный характер и не заменяет консультацию врача. Применение метформина у людей без диабета — это применение вне инструкции, требующее обсуждения с лечащим врачом и индивидуальной оценки соотношения польза/риск.



